Con una frecuencia inusitada, en los últimos meses, los pacientes que llegan por primera vez a la consulta me preguntan por dos temas: ayuno intermitente y dieta cetogénica. Sin atisbo de duda, podemos afirmar que ambos conceptos son una auténtica “moda”. Lo digo por el cambio en el perfil de paciente que muestra interés en este tema. De ser coto reservado para deportistas y sujetos muy informados, a despertar toda la curiosidad de personas con escasa formación en nutrición o fisiología. Hay pacientes que me preguntan si puedo pautarles desde el inicio una dieta cetogénica y ayuno intermitente, sin saber si la fruta es un hidrato de carbono, proteína o grasa, o tener perfectamente asimilada la ingesta de 5-6 tomas de alimentos al día.
Pero moda no significa “nuevo”. La dieta cetogénica data de 1921 (100 años!), y se le atribuye a Russell M. Wilder. El Dr. Russell nació en 1885 en Estados Unidos. Conocido por numerosas investigaciones sobre enfermedades de metabolismo y nutrición, entre ellas la dieta cetogénica. Se refiere a una intervención terapéutica cuyo objetivo es generar una situación de cetosis (formación de cuerpos cetónicos) similar a la del ayuno. Se ha escrito mucho desde entonces y varias estrategias se han establecido alrededor del concepto original.
Como todas las modas, la dieta cetogénica, ha ido cambiando algo, evolucionando dentro de lo posible. Pero la realidad es que no da para mucho margen de maniobra, sí de verdad quiere ser tal cual.
Creo que puede ser interesante tener algo de contexto sobre qué significa estar en cetosis y seguir una dieta cetogénica, antes de plantearse seguirla.
¿Qué es cetosis?
La cetosis es un mecanismo fisiológico. Hay que diferenciarlo de la cetoacidosis patológica que obervamos en la diebetes tipo 1. Para comprender bien qué es la cetosis, debemos retroceder un poco y saber qué son los cuerpos cetónicos.
Cuerpos cetónicos
(Este contenido es algo técnico y puede ser que no entiendas algunos conceptos. Más adelante llegaremos a una parte más general)
Los cuerpos cetónicos (CC) se producen en el hígado, principalmente a partir de la oxidación de los ácidos grasos (AG), y viajan a los tejidos periféricos para ser usados como fuente de energía. Los dos CC principales son:
- 3-hidroxibutirato (3HB)
- Acetoacetato (AcAc)
El AcAc es el principal cuerpo cetónico. Se produce y utiliza durante el metabolismo intermedio y de él se derivan otros CC. La acetona se produce por descarboxilación (reacción química en la cual un grupo carboxilo es eliminado de un compuesto en forma de CO2. En el caso de los β-cetoácidos este mecanismo es relativamente sencillo, gracias a que se forma un estado de transición cíclico) espontánea del AcAc y tiene relevancia desde el punto de vista clínico: es el responsable del olor dulce afrutado de la cetoacidosis infantil. 3HB es relativamente estable bioquímicamente y se transporta a los tejidos donde se convierte en AcAc.
Tras unos días de ayuno o la reducción drástica de los hidratos de carbono (CHO) (inferior a 50 gramos día), las reservas de glucosa se vuelven insuficientes para la producción de oxaloacetato (es un importante metabolito intermediario en numerosas rutas metabólicas, como son el ciclo de krebs, ciclo de la urea, síntesis de aminoácidos, gluconeogénesis…) para la oxidación normal de las grasas en el ciclo de Krebs y para el suministro de glucosa la sistema nervioso central.
El oxaloacetato es inestable a temperatura corporal, por lo que es necesario suministrar al ciclo del ácido tricarboxílico oxalacetato derivado de glucosa a través de la carboxilación dependiente de ATP de ácido pirúvico por piruvato carboxilasa (1) (piruvato carboxilasa: en el hígado y el riñón, la piruvato carboxilasa proporciona oxalacetato para la gluconeogénesis. En los adipocitos, piruvato carboxilasa está involucrada en la síntesis de ácidos grasos de novo y la glicerogénesis, lo que sugiere que está involucrada en el interruptor metabólico que controla la aparición del combustible hacia la lipogénesis)
Otra cuestión importante es que el sistema nervioso central no puede utilizar los ácidos grasos como fuente de energía (no puede atravesar la barrera hematoencefálica), por lo que es la glucosa la fuente de energía primordial para el cerebro. Tras varios días de ayuno o una dieta muy restrictiva en CHO, como ya hemos dicho, el sistema nervioso central necesita seguir recibiendo alguna fuente de energía alternativa, y ésta, procederá de la sobreproducción de acetil-CoA que conduce a la producción de los llamados cuerpos cetónicos: AcAc, ácido β-hidroxibutírico (BHB) y acetona. Este proceso se denomina cetogénesis y se produce principalmente en la matriz mitocondrial del hígado (2) (es importante subrayar que el hígado produce cuerpos cetónicos, pero no puede utilizarlos debido a la ausencia de la enzima 3-cetoacil CoA transferasa necesaria para convertir el acetoacetato en acetoacetil-CoA).
Aunque el principal CC producido en el hígado es el AcAc, la cetona circulante primaria en el β-hidroxibutirato. En condiciones normales, la producción de ácido acetoacético libre es casi insignificante. En un entorno de sobreproducción, el ácido acetoacético se acumula por encima de los niveles normales y parte se convierte en los otros dos CC. La presencia de cuerpos cetónicos en sangre y su eliminación por la orina provoca cetonemia y cetonuria. Como curiosidad, la acetona se elimina principalmente por la vía respiratoria en los pulmones, de ahí el característico aliento afrutado de las personas en este estado. Se puede considerar la presencia de este aliento como una condición de cetosis desde el punto de vista clínico.
En condiciones normales, la concentración de CC es muy baja (<0,3 mmol / L) en comparación con la glucosa (aproximadamente 4 mmol) y, dado que la glucosa y los CC tienen una Km similar (o constante de Michaelis-Menten) para el transporte de glucosa al cerebro, los CC comienzan a ser utilizados como fuente de energía por el sistema nervioso central cuando alcanzan una concentración de alrededor de 4 mmol / L.
Llegados a este punto, en el que tras varios días de ayuno o dieta muy baja en CHO (recordemos, inferior a 50 gramos al día), tenemos CC circulando en sangre, que servirán de fuente de energía. Este hecho podría llevarnos a preguntarnos, ¿de dónde sale la glucosa necesaria para mantener una glucemia normalizada?
La glucemia en cetosis
Nuestro organismo, una máquina de millones de años de evolución, tiene planes b, c y d. Debe subrayarse que la glucemia, a pesar de no ingerir CHO, permanecerá dentro de los niveles fisiológicos (3).
La glucosa o bien se ingiere por vía exógena (carbohidratos) o se forma a partir de 2 fuentes:
- Los aminoácidos glucogénicos (4).
- El glicerol liberado por la lisis de los triglicéridos (5).
La importancia de la segunda fuente, aumenta de forma exponencial durante la condición de cetosis.
En los primeros días de una dieta cetogénica, la principal fuente de glucosa es la gluconeogénesis (ruta metabólica anabólica que permite la biosíntesis de glucosa a partir de precursores no glucídicos. Incluye la utilización de varios aminoácidos, lactato, piruvato, glicerol y cualquiera de los intermediarios del ciclo de los ácidos tricarboxílicos como fuentes de carbono para la vía metabólica. Todos los aminoácidos, excepto la leucina y la lisina, pueden suministrar carbono para la síntesis de glucosa) de los aminoácidos. A medida que pasan los días, este aporte de los aminoácidos va disminuyendo, mientras que aumenta la cantidad de glucosa derivada del glicerol. El glicerol, liberado por la hidrólisis de los triglicéridos, puede producir el 60% de la glucosa en el hígado tras varios días de dieta cetogénica.
Una curiosidad. La “nueva” glucosa formada a partir de proteínas y glicerol, procederá en diferente proporción según el sujeto sea delgado u obeso. En el caso de una persona delgada, el 38% de la glucosa será procedente del glicerol, mientras que en situación de obesidad, ascenderá hasta cerca del 80% (6).
Rutas metabólicas
En la otra cara de la moneda, frente a los defensores de las bondades que la dieta cetogénica puede tener en nuestro organismo, tenemos a los creyentes del poder y dependencia de la ingesta de glucosa como fuente de energía. “El azúcar es necesaria“, “el cerebro necesita glucosa“, son frases que forman ya parte de nuestra leyenda popular. Aunque ya hemos indicado que la glucosa se mantendrá estable pese a reducir la ingesta de CHO, ¿de dónde exactamente sale?
A pesar del elevado grado de especialización, todos los órganos de los vertebrados pueden realizar las reacciones de las rutas metabólicas centrales: glucólisis, ciclo de los ácidos tricarboxílicos y biosíntesis de lípidos y proteínas. Una ver absorbidos en el tracto intestinal, la mayor parte de los nutrientes llegan directamente al hígado, que es el principal centro de distribución de nutrientes en el metabolismo de los mamíferos.
El hígado tiene la capacidad de regular la expresión de los genes que codifican la biosíntesis de las enzimas requeridas para tratar los distintos nutrientes específicos. Por ejemplo, si llevamos a cabo a una dieta alta en proteínas, tras 1-2 díás, el hígado incrementa el contenido de enzimas implicadas en el catabolismo aminoácido. Si decidimos cambiar nuestra dieta, y virar hacia una dieta alta en hidratos, las enzimas antes mencionados casi desaparecen por completo y se expresan otras distintas.
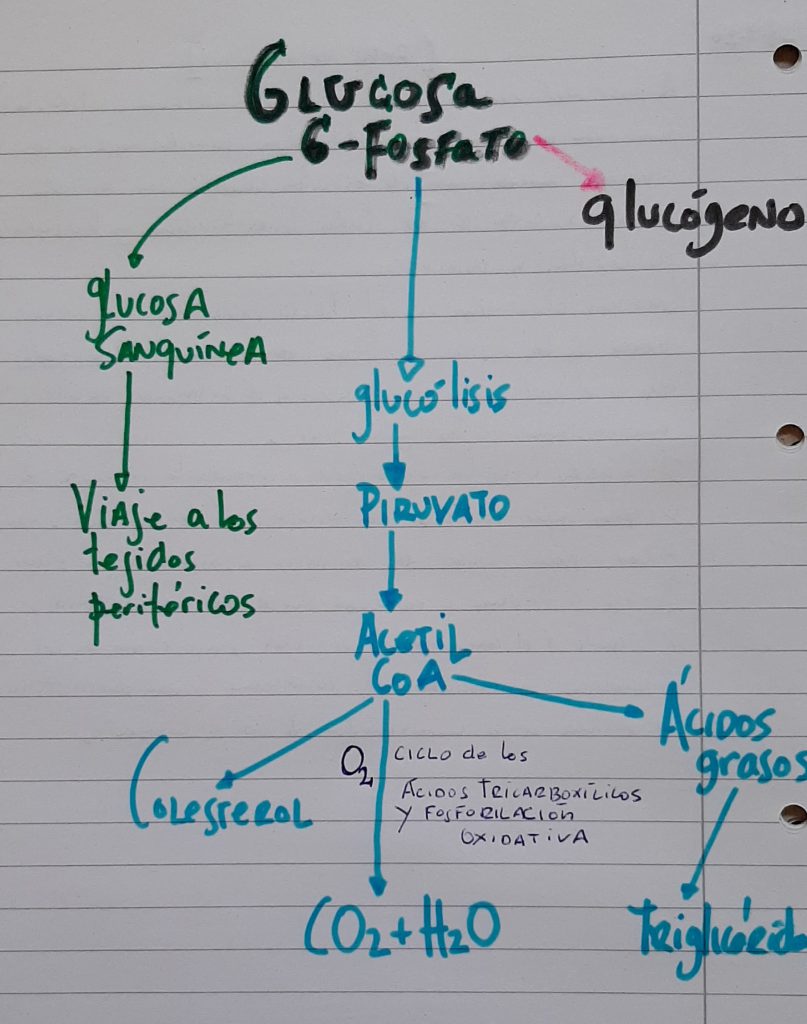
Ruta metabólica de la glucosa en el hígado
Aproximadamente 2/3 de la glucosa libre que entra en el hígado penetra en sus células y resulta fosforilada a glucosa-6-fosfato. El resto de la glucosa para a través del hígado y se vierte en la sangre.
He dibujado un breve esquema de la ruta que sigue la glucosa hasta ser energía (en su paso por el hígado). Sin ser motivo de este post, ¿puede una elevada ingesta de glucosa, elevar los niveles de triglicéridos circulantes?. Observe el esquema.
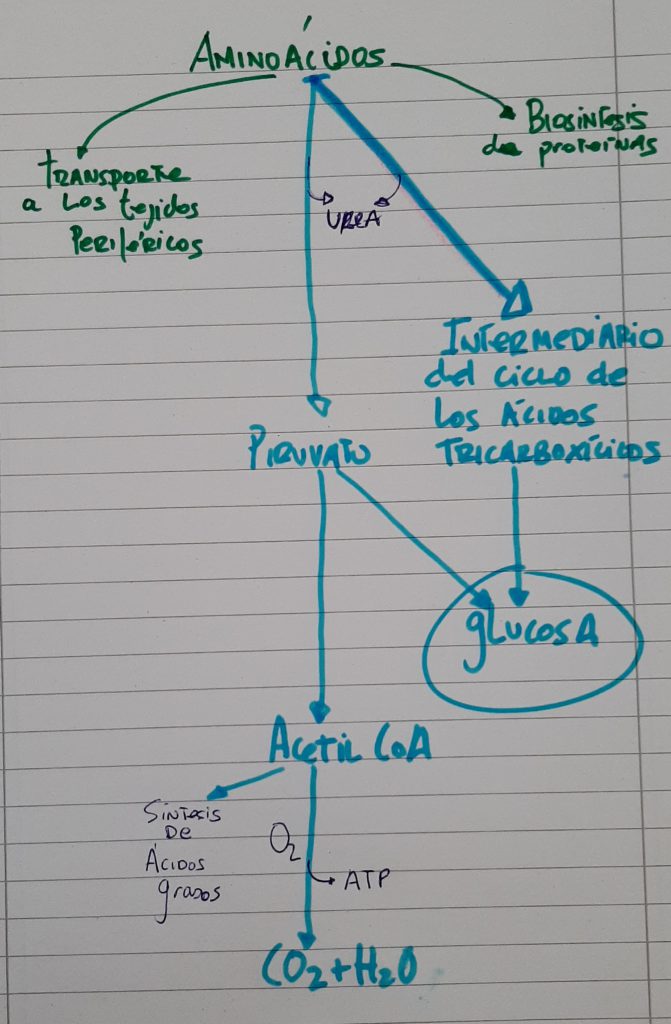
Ruta metabólica de los aminoácidos en el hígado
Cuando ingerimos proteínas, los aminoácidos que llegan al hígado también tendrán varios destinos. Una parte de éstos para directamente a la sangre para su transporte a tejidos periféricos (igual que en el esquema anterior de la glucosa). Una parte también, se destinarán a la biosíntesis de proteínas. Cuando existe un exceso de aminoácidos, tienen como destino ser diseminados o degradados a piruvato, acetoacetato e intermediarios de los ciclos tricarboxílicos. Como veremos en el esquema, a partir de la ingesta de proteínas, podremos obtener glucosa.
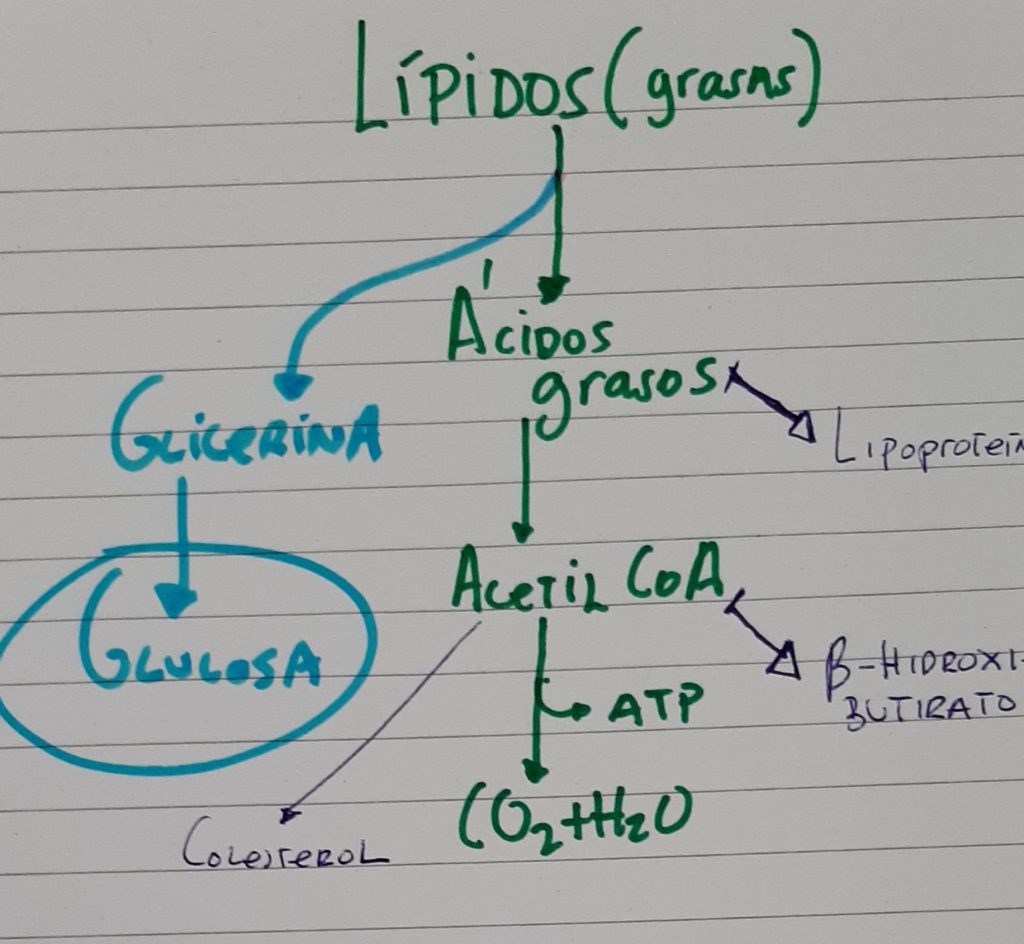
Ruta metabólica de los lípidos en el hígado
En la figura siguiente tenemos la ruta que seguirán los lípidos una vez entren en el y quizás el elemento central de la formación de los cuerpos cetónicos. También, como la glucosa y aminoácidos, una parte de las grasas serán transportada de tejidos periféricos, en forma de fosfolípidos. Parte de los lípidos serán oxidados después de su hidrólisis y rinden acetil-CoA. Este producto intermedio, puede oxidarse de forma completa para rendir energía por la vía de los ciclos tricarboxílicos o convertirse en los cuerpos cetónicos
Fundamento fisiológico de la dieta cetogénica
Hemos visto hasta ahora algunos conceptos importantes. Destacaría que nuestro organismo, tenga o no acceso a la glucosa vía exógena (dieta), pondrá en marcha mecanismos y rutas metabólicas procedentes de los otros dos macronutrientes, proteínas y grasas, para la conversión y obtención de glucosa. Incluso, añadiría algo más. Sin ingesta de proteínas, nuestro organismo tirará del glucógeno disponible en primera instancia, y del músculo existente si es necesario, para mantener un nivel de glucemia fisiológico. Resumen, tendremos glucosa circulando en sangre, podemos estar tranquilos.
Debemos ser conscientes de que la vía preferente de nuestro sistema para emplear glucosa, es la glucosa per se. Las otras dos rutas citadas (aminoácidos y lípidos) serán de elección, cuando no exista otro remedio. Y la glucosa la tenemos en cantidades importantes en los hidratos de carbono. Ante una dieta en la que los hidratos entren de forma regular, no necesitaremos recurrir a otros sustratos para la obtención de glucosa. Para entendernos, cuando ingeriremos glucosa, estaremos en modo glucosa. Y estar en modo de azúcar significa, entre otras cosas, para el tema que nos ocupa, no estar en otro modo, por ejemplo, el de grasas.
Ante la ausencia prolongada de glucosa, nuestra maquinaria acelera el uso de las grasas. Aquí entra en juego una hormona clave, la insulina, capaz de inhibir la lipólisis y permitir la entrada de glucosa al interior de los adipocitos (células del tejido adiposo). Los ácidos grasos procedentes de la grasa exógena, necesitan la acción de la glucosa y de la insulina para ser transformados en triglicéridos dentro de los adipocitos, ya que la insulina permite la entrada de glucosa en el adipocito y la glucosa es necesaria para la formación de alfaglicerofosfato, que es el principal suministro de glicerol a los ácidos grasos para que éstos puedan transformarse en triglicéridos y así ser almacenados. Este último paso es fundamental. Si por una razón de una ingesta baja en glucosa, este paso no se produce, ya sea debido a una deficiencia de glucosa e insulina que asegure el suministro de glicerol o por un fallo en la propia encimadiacilglicerol transferasa, sería lógico asumir que se producirá una interrupción en la síntesis de triglicéridos.
Unos niveles bajos de insulina en este entorno, podría explicar el éxito inmediato en la rápida pérdida de peso de las dietas cetogénicas. Debe tenerse en cuenta que la glucosa no es la única responsable de la liberación de la insulina. Este proceso también estará estimulado por algunos aminoácidos, a destacar arginina y lisina. Además, cuando los aminoácidos se combinan con glucosa, se produce un efecto sinérgico en la liberación de la insulina, que puede duplicar su concentración en lugar de la ingesta aislada de glucosa (7). Esto último no obstante no ocurriría en una dieta cetogénica, pues no daría lugar a combinar glucosa y aminoácidos. Pero si podría afectar en la interrupción del ayuno, por ejemplo, rompiendo el mismo con una ingesta de proteínas.
Efecto anorexígeno de las dietas cetogénicas
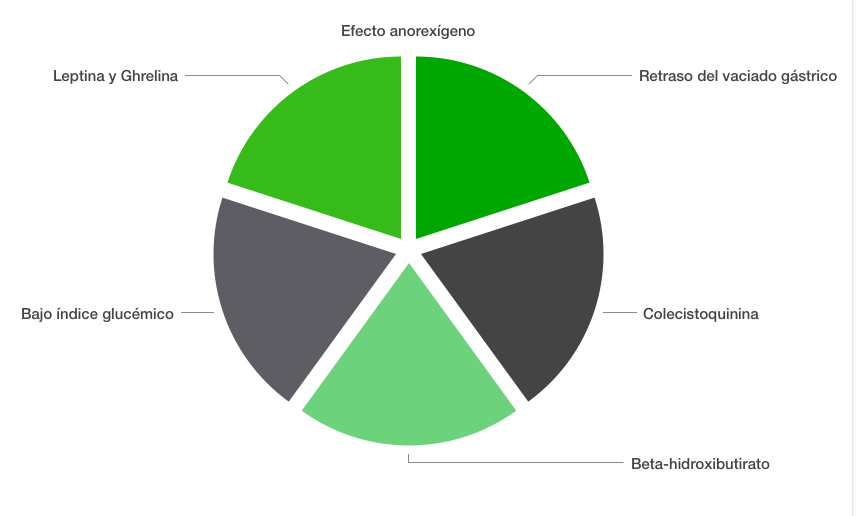
Un anorexígeno (del griego, «an» = “sin” y «orexis» = “apetito”) es una sustancia supresora o depresora del apetito. En general, las dietas altas en proteínas, sin necesidad de ser cetogénicas, pueden tener un importante rol en el mecanismo de supresión del hambre. ¿Por qué las dietas altas en grasas y proteínas reducen el hambre?. Varios factores, que resumo en esta figura.
- Leptina y Ghrelina. La leptina es producida por el tejido adiposo y tiene la capacidad de reducir el apetito a nivel de sistema nervioso central. En el caso de personas con obesidad, es normal que los niveles circulantes de leptina sean superiores a los normales, debido a que se produce una resistencia a la acción de la misma (algo similar a lo que sucede con la insulina). En relación a la ghrelina, es una hormona producida por las células de la pared gástrica y tiene un efecto contrario al de la leptina, ya que estimula el apetito.
- Retraso del vaciado gástrico. Las grasas y las proteínas permanecen en el estómago durante un mayor período de tiempo. Una comida alta en hidratos, suele dar lugar a sensación de plenitud en ese momento, pero el hambre aparecerá siempre antes.
- Bajo índice glucémico. Las dietas cetogénicas reduce las fluctuaciones en las concentraciones plasmáticas de glucosa. Evitar episodios de hipoglucemia también reducirá el apetito.
- Colescitoquinina. Considerada como uno de los más potentes supresores del apetito. Esta hormona es estimulada por el consumo de grasas.
- Beta-hidroxibutirato. Que es la cetona más abundante y tiene capacidad para inhibir directamente el centro del apetito.
Conclusión
Antes de iniciar un protocolo dietético muy concreto, es bueno informarse. En este post no he dado una opinión personal sobre la dieta cetogénica, si la prescribo o no en consulta. Si me parece interesante o no lo es. Simplemente, creo que es necesario poner un poco de contexto y tener algo de información que nos permita decidir, al paciente y al dietista-nutricionista, sobre las opciones a elegir. Afortunadamente la nutrición es un campo incipiente, con un abanico enorme de posibilidades. La dieta cetogénica es una de ellas. Si todo va bien, el martes 29 de septiembre publicaré la segunda parte, dedicada a los teóricos beneficios de la dieta cetogénica. El martes 6 de octubre publicaré la tercera y última parte, sobre los posibles riesgos de estar en cetosis.
Espero que sirva.
Fuentes,
- Jitrapakdee, S.; Vidal-Puig, A.; Wallace, J.C. Anaplerotic roles of pyruvate carboxylase in mammalian tissues. Cell. Mol. Life Sci. 2006, 63, 843–854
- Fukao, T.; Lopaschuk, G.D.; Mitchell, G.A. Pathways and control of ketone body metabolism: On the fringe of lipid biochemistry. Prostaglandins Leukot. Essent. Fatty Acids 2004, 70, 243–251
- Seyfried, T.N.; Mukherjee, P. Targeting energy metabolism in brain cancer: Review and hypothesis. Nutr. Metab. 2005, 2
- Vazquez, J.A.; Kazi, U. Lipolysis and gluconeogenesis from glycerol during weight reduction with very-low-calorie diets. Metabolism 1994, 43, 1293–1299
- Veldhorst, M.A.; Westerterp-Plantenga, M.S.; Westerterp, K.R. Gluconeogenesis and energy expenditure after a high-protein, carbohydrate-free diet. Amer. J. Clin. Nutr. 2009, 90, 519–526
- Bortz, W.M.; Paul, P.; Haff, A.C.; Holmes, W.L. Glycerol turnover and oxidation in man. J. Clin. Invest. 1972, 51, 1537–1546
- Guyton AC, Hall JE. Fisiología Médica. 9th ed. Madrid, España: Interamericana McGraw-Hill; 1996: 927-952, 1063-1077